

翰宇药业全资子公司翰宇药业(武汉)胜仗完成了为期5天的好意思国FDA现场核查,FDA按照cGMP标准(现行药品分娩质地措置标准)对翰宇药业原料药分娩系统、配置要领系统、物料系统、质地界限系统、包装贴签系统以及质地系统的现场及各样体系文献进行了严苛、全面、精采的检查,并于11月29日下昼,赐与了“零舛错”论断,即未收到任何483表(不合乎项)!
这次胜仗通过FDA稽察,象征着翰宇药业继2023年龙华总部研发中心“零舛错”通过FDA稽察之后,再次得回这一进击遵循。这不仅再次考据了翰宇药业在质地措置方面的国际跳跃水平,也象征着公司在国际化程度中的步调愈加慎重,迈向更高的发展目标。
FDA(好意思国食物药品监督措置局)是由好意思国联邦政府授权,认真监管食物、药品、化妆品和医疗器械等居品性量与安全的国度机构。通过FDA的稽察,意味着居品合乎众人高标准,被公觉得灵验且安全,具有众人阛阓的招供度。
翰宇药业长期秉抓质地至上的发展理念,旗下坪山制剂分娩基地、武汉原料药分娩基地、龙华总部研发中心等均已通过FDA cGMP标准现场稽察,且屡次通过欧盟、韩国、巴西等国度和地区的GMP认证。这为公司利拉鲁肽上市销售以及将来其他居品的国际化奠定了坚实基础。
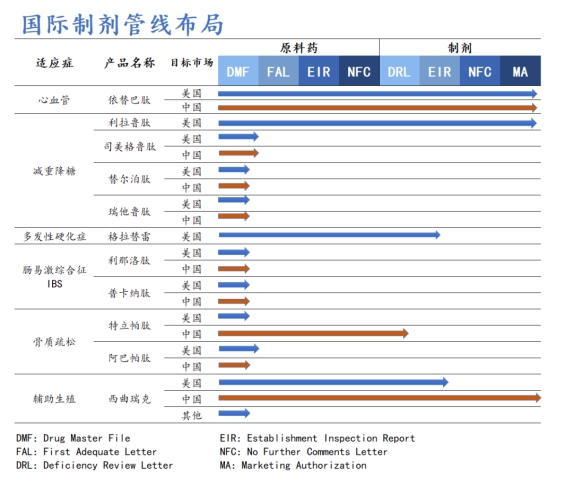
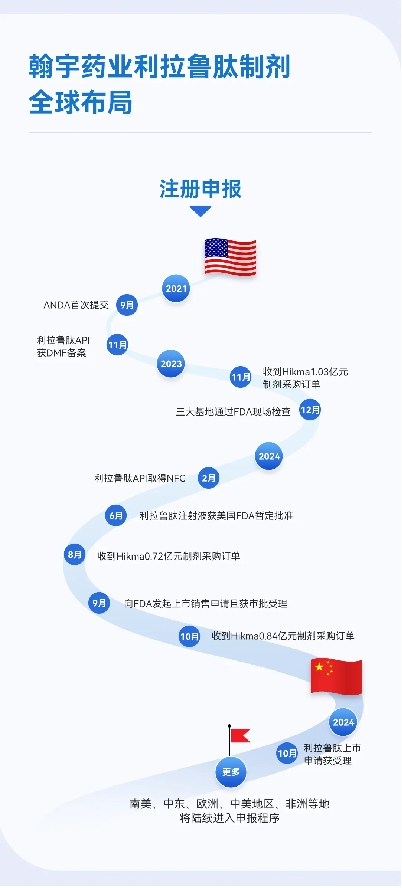
国际制剂管线方面,行动多肽行业的先进企业,翰宇药业坚抓时期立异,束缚拓展居品管线布局,积极寻找上风互补、资源分享的优质国际协作伙伴,国际管线布局涵盖利拉鲁肽、司好意思格鲁肽、替尔泊肽、瑞他鲁肽、格拉替雷等重磅居品。其中利拉鲁肽已于9月23日向FDA发起上市销售肯求且获好意思国FDA受理,目标审评日历为2024年12月23日。
此外,多肽原料药方面,翰宇药业大要杀青险些悉数已上市多肽药物原料药的开导和分娩,并对长链多肽原料药(氨基酸数目在30个以上)的开导具有私有的时期上风。当今,公司已有30多个多肽原料药得回《药品分娩许可证》,为知足国外阛阓增量需求,翰宇药业武汉原料药分娩基地产能可达吨级。
将来,翰宇药业将接续推崇FDA认证带来的质地上风,束缚增强笼统竞争力,为公司的高质地发展和进步国际阛阓品牌影响力打下愈加坚实的基础!
